以下为整合多个优质教学资源后设计的氧化还原反应教案框架,适用于公开课教学,兼顾知识进阶与核心素养培养:
一、教学目标
1. 知识与技能
理解氧化还原反应的特征(化合价升降)与本质(电子转移)。
掌握用双线桥法标注电子转移的方向和数目,区分氧化剂与还原剂。
能基于化合价变化判断反应是否为氧化还原反应,并分析其应用场景(如金属冶炼、能量转化)。
2. 过程与方法
通过实验探究(如钠与反应、锌铜原电池)理解电子转移的微观本质。
运用分类与比较方法,辨析四种基本反应类型与氧化还原反应的关系。
构建“宏观现象→化合价变化→电子转移”的认知模型,形成科学思维。
3. 情感态度与价值观
体会对立统一规律(氧化与还原共存),培养辩证唯物主义观。
通过氧化还原反应在生活中的应用(如电池、金属防腐),感悟化学的社会价值。
二、教学重难点
重点:
氧化还原反应的特征(化合价升降)与本质(电子转移)的关联。
双线桥法的规范使用及氧化剂/还原剂的判断。
难点:
从微观电子转移角度解释化合价变化的本质。
氧化还原反应与能量转化的关系(如原电池原理)。
三、教学过程
环节1:情境导入,引发认知冲突
活动设计:
展示铁生锈、食物腐败等生活现象,提问:“这些反应是否属于氧化还原反应?”。
回顾初中知识:学生列举得氧/失氧的氧化还原反应实例(如C还原CuO),讨论分类标准的局限性。
问题链:
“若反应无氧气参与(如Zn与CuSO₄反应),如何判断是否为氧化还原反应?”。
环节2:进阶探究——从化合价到电子转移
1. 宏观特征分析
任务:标出Fe + CuSO₄ → FeSO₄ + Cu反应中各元素的化合价,总结“凡有化合价升降的反应均为氧化还原反应”。
对比实验:分析NaCl(离子键)与HCl(共价键)的形成过程,通过原子结构示意图解释电子得失或偏移如何导致化合价变化。
2. 微观本质揭示
实验探究:
钠与燃烧实验(观察现象,结合动画演示电子转移过程)。
锌铜原电池实验(检流计指针偏转验证电子转移)。
模型建构:
双线桥法示范:以2Na + Cl₂ → 2NaCl为例,标注电子转移方向与数目,总结“失升氧,得降还”规律。
环节3:深化理解——对立统一与分类应用
辩证关系讨论:
以H₂ + Cl₂ → 2HCl为例,分析氧化与还原的共存性,强调反应中的对立统一。
分类与迁移:
绘制维恩图,展示四大基本反应类型与氧化还原反应的交叉关系。
案例分析:光合作用、金属冶炼等实际应用中的氧化还原反应。
环节4:巩固与评价
分层练习:
1. 基础题:判断反应是否为氧化还原反应(如分解H₂O₂、酸碱中和)。
2. 进阶题:用双线桥法分析KMnO₄分解反应中的电子转移。
反思总结:学生提炼知识框架,教师强调电子转移是本质,化合价变化是表象。
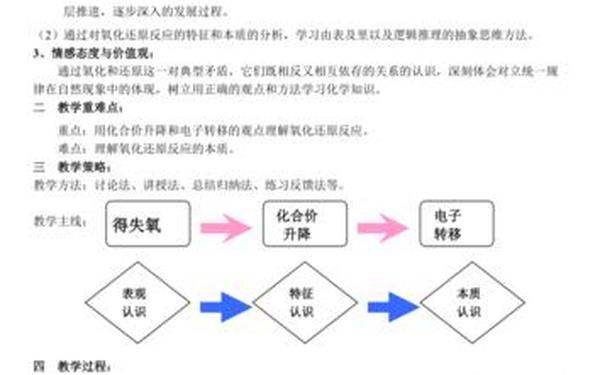
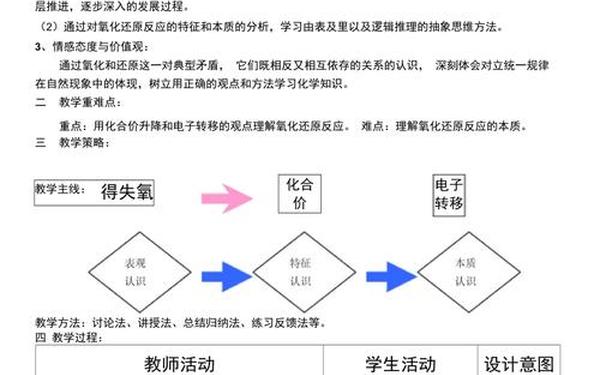
四、板书设计
氧化还原反应
一、特征:化合价升降
二、本质:电子转移(得失或偏移)
三、模型:
失e⁻ → 化合价↑ → 氧化反应(还原剂)
得e⁻ → 化合价↓ → 还原反应(氧化剂)
四、应用:能量转化、物质制备
五、教学特色
1. 实验驱动:通过原电池实验直观验证电子转移,突破抽象难点。
2. 哲学渗透:以“对立统一”串联氧化与还原的关系,深化学科育人价值。
3. 进阶设计:从生活现象到微观本质,层层递进构建认知模型。
参考资料:教学设计综合自网页1、15、32、46、75等,实验设计参考网页46的原电池探究,哲学思想部分借鉴网页32的辩证分析。



